
Méhméreg: mit mond a tudomány a gyulladásról, a fájdalomról, a bőrről és a jövő terápiáiról?
Méhméreg (apitoxin): mit mond a modern tudomány a gyulladásról, a fájdalomról, a bőrről és a jövő terápiáiról?
Hosszú, bizonyítéksúlyozott összefoglaló a méhméreg összetételéről, feltételezett és igazoltabb pozitív hatásairól, valamint a klinikai korlátokról, a topikális készítményekről és a biztonsági kérdésekről.
Gyors válasz
A méhméreg (apitoxin) tudományos megítélése óvatosan biztató, de nem korlátlanul pozitív. A ma legerősebb humán jelek elsősorban bizonyos mozgásszervi fájdalomállapotok és egyes bőrgyógyászati alkalmazások felé mutatnak, miközben a neuroprotektív, antivirális és onkológiai irányok nagy része továbbra is preklinikai kutatási szakaszban van. Méhmérges krémeink.
A legfontosabb gyakorlati üzenet: a topikális méhméreges készítmények és az injekciós apiterápiás megközelítések nem ugyanazt jelentik sem hatásban, sem kockázatban. A természetes eredet nem egyenlő automatikus biztonsággal: az allergia, az irritáció és ritka esetben az anafilaxia kockázata miatt a méhméreg értékelése csak a bizonyítékok és a biztonsági szempontok együtt mérlegelésével korrekt.
Kivonat. A méhméreg (apitoxin) a modern kutatásban egyre fontosabb természetes bioaktív rendszerként jelenik meg. Fő komponensei - különösen a melittin, a foszfolipáz A2, az apamin és az adolapin - gyulladásos, fájdalmi, immunológiai és bőrbiológiai folyamatokra hathatnak. A humán bizonyítékok jelenleg legerősebben bizonyos mozgásszervi fájdalomállapotok és néhány bőrgyógyászati alkalmazás irányában mutatnak, miközben a neuroprotektív, antivirális és onkológiai vonal döntően preklinikai szakaszban van. A méhméreg kutatási és gyakorlati értékét ugyanakkor alapvetően korlátozza az allergiakockázat, a dózisfüggő citotoxicitás és a készítmények heterogenitása. Ez az áttekintés a 2026. március 11-ig elérhető főbb szakirodalom alapján foglalja össze a méhméreg összetételét, hatásmechanizmusait, pozitív hatásait, kockázatait, valamint a topikális készítmények és az injekciós alkalmazások közötti különbségeket[1], [2], [5], [7], [12], [19], [21], [22], [23].
Kulcsszavak: méhméreg, apitoxin, melittin, foszfolipáz A2, méhméreg hatása, méhméreg pozitív hatásai, méhméreg krém, méhméreg kenőcs, apiterápia, gyulladáscsökkentés, fájdalomcsillapítás, bőrápolás.
Legerősebb humán jel
Mozgásszervi fájdalom és bizonyos bőrgyógyászati alkalmazások.
Legfontosabb molekula
A melittin, de a teljes hatás sosem szűkíthető egyetlen komponensre.
Legnagyobb kockázat
Allergia és anafilaxia - a természetes eredet nem kockázatmentesség.
Legfontosabb tanulság
Topikális krém és injekciós beavatkozás nem ugyanaz a farmakológiai történet.
Bevezetés és olvasói gyorskalauz
A méhméreg - tudományos nevén apitoxin - egyszerre tartozik a hagyományos apiterápia legismertebb anyagai és a modern farmakológia legizgalmasabb természetes kutatási modelljei közé. Kevés olyan méhészeti eredetű anyag van, amelyet ennyire különböző nézőpontból vizsgálnának: a bőrgyógyászattól a fájdalomkutatáson át a neuroimmunológiáig. A szakirodalom alapján a méhméregben található peptidek, enzimek és kis molekulák több jelátviteli útvonalba is beleszólnak, különösen a gyulladás, a fájdalomérzet és az immunválasz szabályozásában[1], [2], [3], [4].
Ugyanakkor már az elején érdemes tisztázni a legfontosabb szakmai keretet: a méhméreggel kapcsolatban sok az ígéret, de nem minden terület egyformán bizonyított. A legerősebb humán adatok ma elsősorban bizonyos mozgásszervi fájdalomkórképek és néhány bőrgyógyászati alkalmazás körül gyűlnek, miközben a Parkinson-kórral, a fertőzésekkel vagy az onkológiával kapcsolatos eredmények döntő többsége még preklinikai szinten van. Más szóval: a méhméreg nem csodaszer, hanem egy komplex bioaktív rendszer, amelynél az alkalmazás módja, a dózis, a tisztaság és a beteg kiválasztása mindent meghatároz[2], [4], [5], [7].
Ez a cikk nem szó szerinti fordítás és nem reklámszöveg, hanem egy hosszú, hivatkozott, bizonyítéksúlyozott áttekintés. Kifejezetten arra készült, hogy blogcikként is olvasható legyen, mégis megőrizze egy nyomtatott tudományos összefoglaló fegyelmét. A fő cél kettős: egyrészt megmutatni, milyen pozitív hatásokat tár fel a szakirodalom a méhméreg kapcsán, másrészt világosan leírni a korlátokat, a biztonsági kérdéseket és azt, hogy egy méhméreges krém vagy kenőcs nem azonos az injekciós, klinikai környezetben végzett beavatkozásokkal[2], [6], [8], [12], [21], [22].
Ha a tudományos háttér mellett a topikális termékek világa is érdekli, érdemes külön átnézni a méhméreg és méhmérges kenőcsök kategóriáját, ahol a bőrre szánt készítmények szempontjai más logika szerint értelmezendők, mint az injekciós vagy akupunktúrás irodalom. Ez a különbségtétel azért kulcsfontosságú, mert a Google és az olvasó is azt szereti, ha egy cikk nem összemossa, hanem tisztán szétválasztja az eltérő felhasználási formákat.
- A méhméreg legnagyobb mennyiségű bioaktív komponense általában a melittin, de a foszfolipáz A2, az apamin, az adolapin és a hialuronidáz is fontos szereplő.
- A legerősebb humán bizonyítékok ma a fájdalom és egyes gyulladásos állapotok területén látszanak, de a hatás erősen függ az alkalmazás módjától.
- A topikális méhméreges kozmetikumok és kenőcsök eredményei nem azonosíthatók automatikusan az injekciós méhméreg-terápiával.
- A bőrgyógyászati és kozmetológiai vonal ígéretes, különösen atópiás dermatitisz és bőrtextúra kapcsán, de a formuláció minősége mindent meghatároz.
- Onkológiai, antivirális és neuroprotektív téren sok a preklinikai adat, ám ezek még nem egyenértékűek a rutin klinikai felhasználással.
- A legnagyobb kockázat továbbra is az allergia és az anafilaxia lehetősége. A 'természetes' nem jelent automatikus biztonságot.
Hogyan készült ez az áttekintés?
Módszertani megjegyzés. Ez az anyag narratív, bizonyítéksúlyozott szakirodalmi áttekintés. A cikk elkészítésekor elsőbbséget kaptak a szakfolyóiratban megjelent áttekintések, randomizált vizsgálatok, szisztematikus áttekintések, metaanalízisek és az allergológiai irányelvek. Külön figyelmet kapott az, hogy az állatkísérletes és sejtbiológiai eredmények ne keveredjenek össze a humán alkalmazhatósággal[1], [2], [5], [7], [9], [21], [22].
A szakmai súlyozásnál négy kérdésre kerestük a választ. Egy: milyen erős a humán bizonyíték? Kettő: mennyire reprodukálhatók a mechanisztikus eredmények? Három: mennyire standardizálható a készítmény? Négy: mekkora a valós életbeli kockázat, különösen az allergia szempontjából? Ez a négyes szűrő azért fontos, mert a méhméreggel kapcsolatos állítások gyakran ott csúsznak meg, hogy laboratóriumi eredményt klinikai ígéretként kommunikálnak.
Az áttekintés időhatára a cikk lezárásának napja: 2026. március 11. Ahol frissebb, 2024-2025-ös összefoglalók álltak rendelkezésre, ott azokat is beépítettük, különösen a farmakológiai mechanizmusok, a mozgásszervi fájdalom és a biztonság kérdésében[2], [7], [23].
Történeti háttér: hagyományból a laboratóriumig
A méhméreg története jóval régebbi, mint a modern farmakológia. A hagyományos apiterápiás rendszerekben a méhészeti eredetű anyagokat - méz, propolisz, méhpempő, virágpor és méhméreg - évszázadok óta különféle célokra használták. A modern tudomány számára azonban a fordulópontot nem maga a hagyomány jelentette, hanem az, amikor a méhméreg összetevőit elkezdték izolálni, meghatározni és mechanisztikusan vizsgálni. A hangsúly ezzel átkerült a 'népi tapasztalatról' a molekuláris, immunológiai és klinikai értelmezésre[1], [2], [3], [4].
Ez a váltás azért fontos, mert a mai olvasó egyszerre találkozik történeti romantikával és modern biomolekuláris nyelvvel. A két világ nem zárja ki egymást, de nem is azonos. Attól, hogy egy anyagot régóta ismer a hagyomány, még nem válik automatikusan bizonyítottá; ugyanakkor attól sem érdektelen, hogy a modern klinikai adatok még nem minden indikációban erősek. A méhméreg esetében a hagyomány inkább hipotézisforrásnak tekinthető, amelyet a laboratóriumi és humán vizsgálatok fokozatosan szűrnek meg[2], [4], [5].
Az elmúlt két évtized kutatásai különösen azért gyorsultak fel, mert a melittin, a PLA2 és más komponensek kapcsán egyre több jelátviteli, sejtmembrán- és immunmodulációs összefüggés vált láthatóvá. A mai publikációk már nem csak azt kérdezik, hogy 'hasznos-e a méhméreg', hanem azt, hogy a teljes venom vagy annak egyes frakciói milyen fejlesztési pályán vihetők tovább. Ez a gondolkodás sokkal közelebb áll a korszerű gyógyszerkutatáshoz, mint a klasszikus apiterápiás szóhasználathoz[1], [2], [3], [19].
Mi az a méhméreg (apitoxin)?
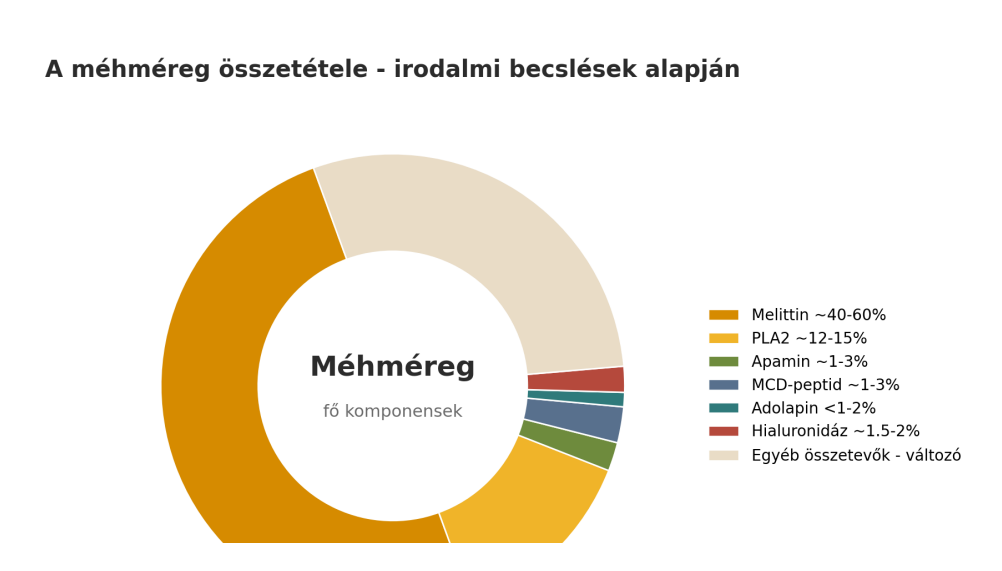
A méhméreg a háziméh, leggyakrabban az Apis mellifera védekező váladéka. Nem egyetlen 'hatóanyag', hanem több tucat biológiailag aktív komponensből álló keverék. A legismertebb összetevő a melittin, amely a legtöbb összetételi becslés szerint a szárazanyag nagyjából 40-60%-át adhatja. Emellett jelentős a foszfolipáz A2 (PLA2) aránya is - gyakran 12-15% körül említik -, továbbá jelen vannak olyan kisebb, de biológiailag fontos peptidek és enzimek, mint az apamin, az adolapin, a mast cell degranulating peptide (MCD-peptid) és a hialuronidáz[1], [2], [3], [4].
A köznyelv sokszor egységesen 'méhméregként' hivatkozik minden felhasználásra, a kutatás azonban legalább négy eltérő kontextust különít el: az eredeti méhcsípés biológiáját, a standardizáltan gyűjtött és feldolgozott nyers méhmérget, a klinikumban vizsgált injekciós vagy pharmacopuncture jellegű készítményeket, valamint a kozmetikai vagy bőrápolási célra formált topikális termékeket. Ugyanarról az alapanyagról beszélünk, de nem ugyanazokról a kockázatokról, felszívódási útvonalakról és bizonyítékokról[2], [4], [5], [12].
A modern gyűjtés tipikusan enyhe elektromos ingerléssel történik: a méhek egy üveglapra vagy gyűjtőfelületre csípnek, ahol a venom megszárad, majd összegyűjthető. A szakirodalom szerint ennél a módszernél a méh nem veszti el a fullánkját, és az eddigi megfigyelések alapján a termelékenységre vagy az áttelelésre nincs feltétlenül káros, egyértelműen kimutatható hatás, bár a folyamat mérsékelt stresszválasszal járhat. Ez a rész azért fontos, mert a fenntarthatóság és az állatjólét ma már a tudományos és a vásárlói bizalomnak is része[2], [4].
Egy természetes méhcsípés során a befecskendezett venom mennyisége legfeljebb néhány tized milligramm - gyakran legfeljebb körülbelül 0,3 mg - lehet, miközben a készítményekben használt koncentrációk, tisztasági fokok és vivőanyagok ettől jelentősen eltérhetnek. Éppen ezért a 'méhméreg hatása' mindig csak az alkalmazás módjával együtt értelmezhető. A laikus kérdés, hogy 'jó-e a méhméreg?', tudományos nyelvre lefordítva így hangzik: melyik összetevő, milyen formulában, milyen indikációban, milyen dózisban, mennyire biztonságosan?[2], [3], [4], [21], [22].
A méhméreg fő komponensei
A méhméreg kutatási értéke éppen a komplexitásában rejlik. Nemcsak arról van szó, hogy több aktív anyag található benne, hanem arról is, hogy ezek egymás hatását módosíthatják. A melittin például erős membránaktivitással rendelkezik, pórusképző tulajdonságú, ezért egyszerre kapcsolják össze antimikrobiális és tumorsejt-ellenes megfigyelésekkel, ugyanakkor a dózisfüggő citotoxicitás miatt a fejlesztések egyik nagy kérdése, hogyan lehet a kedvező hatásokat úgy megtartani, hogy a károsodást visszaszorítsák[1], [2], [3], [19].
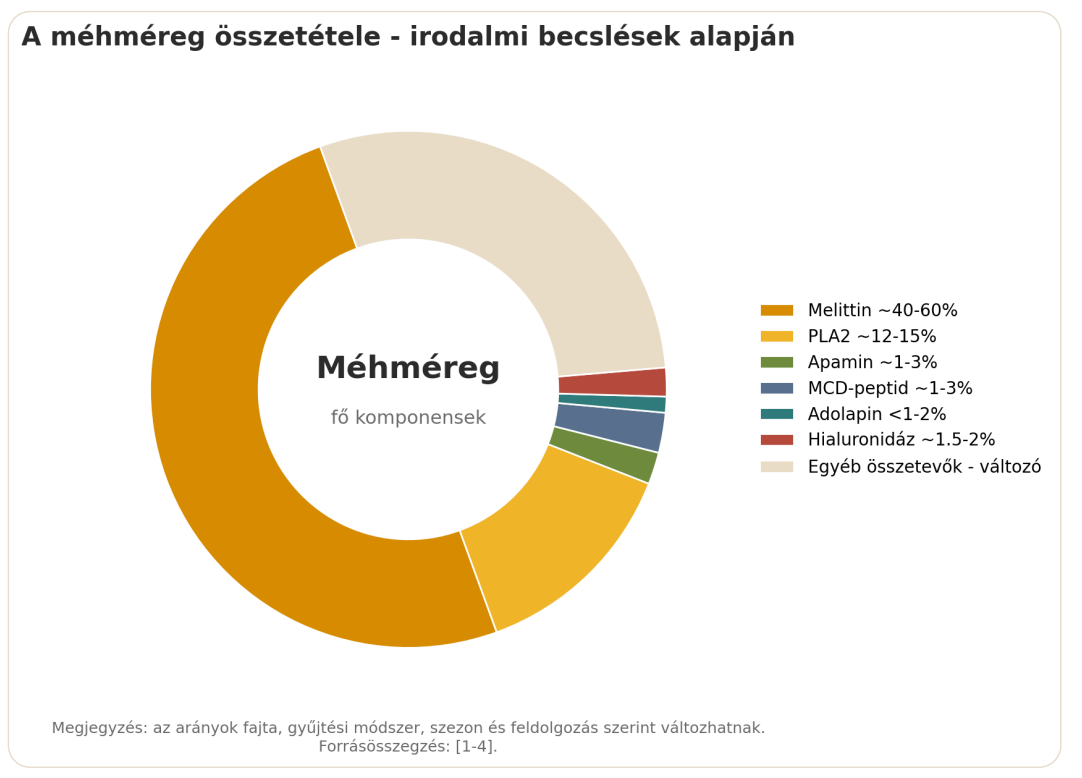
A foszfolipáz A2 különösen érdekes kettős szereplő. Egyrészt az allergiás reakciók egyik fontos fehérjéje, másrészt több preklinikai modellben immunmoduláló, sőt neuroprotektív irányú hatást tulajdonítanak neki. Ez a kettősség jól mutatja, miért félrevezető a méhméregre úgy tekinteni, mintha az csupán 'gyulladáscsökkentő' vagy pusztán 'veszélyes' lenne. Valójában egy biológiailag sokarcú anyagról beszélünk[1], [2], [16], [21], [23].
| Komponens | Jellemző arány | Főként vizsgált hatás | Klinikai jelentőség röviden |
|---|---|---|---|
| Melittin | kb. 40-60% | Membránhatások, gyulladásos jelátvitel modulálása, antimikrobiális és citotoxikus aktivitás | A méhméreg legismertebb molekulája, de kettős természetű: magasabb dózisban irritáló és sejtkárosító lehet, alacsonyabb dózisban viszont több vizsgálat gyulladáscsökkentő irányú mechanizmust ír le. |
| Foszfolipáz A2 (PLA2) | kb. 12-15% | Immunmoduláció, neuroinflammáció, allergén szerep | Egyszerre fontos kutatási célpont és jelentős allergén. A neuroimmunológiai irodalomban különösen sokat vizsgált komponens. |
| Apamin | kb. 1-3% | SK-csatornák modulálása, neurofiziológiai hatások | Főként idegrendszeri modellekben érdekes; humán terápiás következtetésre egyelőre kevés az adat. |
| Adolapin | <1-2% | Fájdalom és gyulladás mediátorainak befolyásolása | Történetileg fontos peptid, de a modern klinikai irodalomban ritkábban kerül önálló fókuszba. |
| Hialuronidáz | kb. 1.5-2% | Szöveti terjedés, allergénpotenciál | Az úgynevezett 'spreading factor' szerep miatt fontos, és az allergológiai vonalon külön figyelmet kap. |
A klinikai értelmezés szempontjából az egyik legfontosabb felismerés az úgynevezett bifázisos hatás. Több áttekintés kiemeli, hogy a méhméreg és különösen a melittin magasabb dózisban fájdalmat, viszketést, erythemát és gyulladásszerű reakciót provokálhat, míg alacsonyabb dózisok és jól megválasztott alkalmazási módok esetén antiinflammatorikus jelátvitel is megfigyelhető. A laboratóriumi irodalom ilyen összefüggésben gyakran említi az IL-6, IL-8, TNF-alpha, IFN-gamma, NF-kB, Akt és ERK útvonalakat[1], [2], [4], [11].
Hatásmechanizmusok: gyulladás, fájdalom, immunválasz
A méhméreg pozitív hatásairól szóló szakirodalom egyik közös nevezője a gyulladásos jelátvitel modulálása. A melittin mechanisztikus kutatásaiban visszatérően megjelenik az IKK/NF-kB tengely gátlása, valamint az iNOS- és COX-2-aktivitás csökkenése. Ez azért fontos, mert ezek a csomópontok a gyulladásos mediátorok termelődésének központi szabályozói, vagyis a fájdalom, a duzzanat és a szöveti irritáció mögött álló biokémiai zajt mérsékelhetik[10], [11].
A fájdalomcsillapító potenciál nem merül ki a klasszikus gyulladáscsökkentésben. A fájdalomkutatásról szóló áttekintések szerint a méhméreg-akupunktúra vagy pharmacopuncture hatása perifériás, gerincvelői és központi idegrendszeri szinten is értelmezhető lehet. A jelenlegi tudás alapján ez inkább egy hálózatos mechanizmus, semmint egyetlen 'varázskulcs': gyulladásos mediátorok csökkenése, nociceptív jelátvitel módosulása és leszálló fájdalomgátló rendszerek bevonódása együtt adhatják a megfigyelt eredményt[5], [7], [8].
Az immunmoduláció terén a PLA2 kap sok figyelmet. Preklinikai Parkinson-modellekben például azt figyelték meg, hogy a bvPLA2 fokozhatja a regulátor T-sejtek aktivitását, miközben visszafoghatja a Th1 és Th17 irányú gyulladásos választ. Ez a neuroimmunológiai nézőpont azért különösen izgalmas, mert a jövőben elképzelhető, hogy nem a teljes méhméreg, hanem annak egy-egy tisztított, célzottan alkalmazott frakciója kerül közelebb a terápiás hasznosításhoz[2], [15], [16].
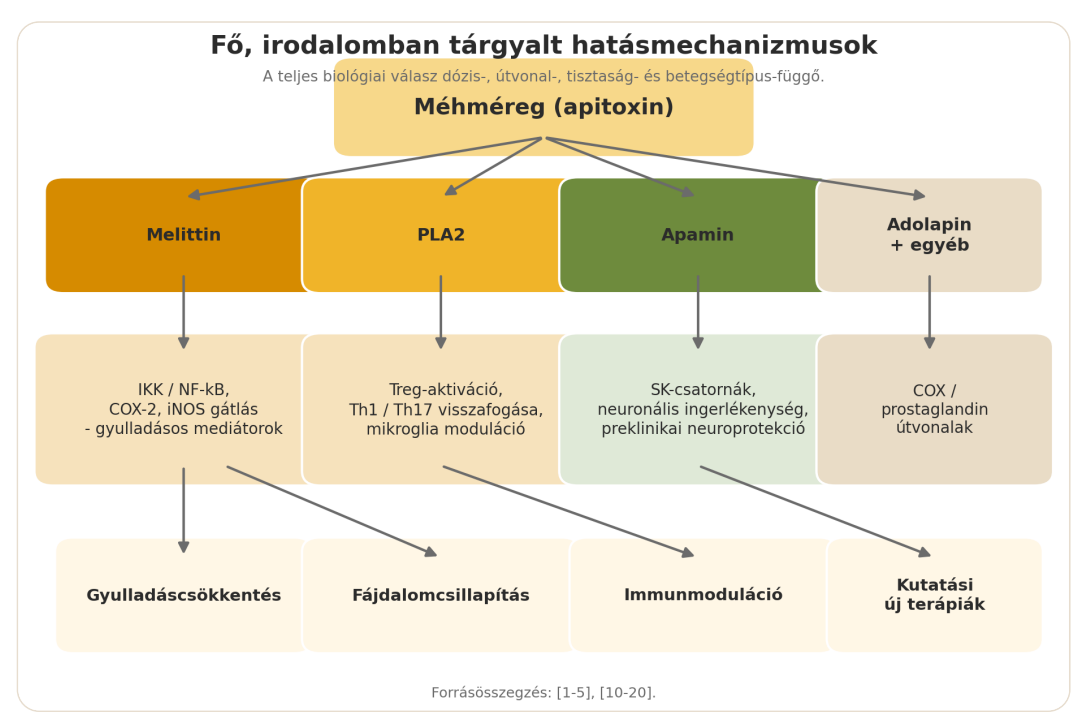
A bőrgyógyászati alkalmazásoknál a mechanizmus gyakran a keratinocyták és immunsejtek közötti gyulladásos kommunikáció csillapításával kapcsolódik össze. Atópiás dermatitisz-modellekben a bee venom és a melittin csökkentette több olyan kemokin és citokin expresszióját, amely az atópiás gyulladás fenntartásában kulcsfontosságú. A bőrgyógyászati irodalom ezért a méhmérget nem egyszerűen 'csípős anyagként', hanem lehetséges jelátviteli modulátorként kezeli[12], [13].
Az onkológiai és fertőzésellenes kutatásokban a membránhatások ismét előtérbe kerülnek. A melittin és egyes méhméreg-frakciók képesek lehetnek tumorsejtek vagy mikroorganizmusok membránjának károsítására, illetve növekedési faktorokhoz kapcsolódó jelátviteli utak megzavarására. Ez azonban éppen azért nehéz fejlesztési terület, mert az egészséges sejtek védelme mellett kell megtartani a szelektív hatékonyságot. Innen ered a nanorészecske-, liposzóma- és célzott vivőrendszerek iránti nagy érdeklődés[2], [17], [18], [19].
Miért ennyire fontos a dózis és az útvonal?
A méhméreggel kapcsolatban talán a dózis a leginkább alábecsült tényező. Ugyanaz az anyag nagyon eltérő biológiai képet adhat attól függően, hogy milyen mennyiségben, milyen időtartam alatt, milyen útvonalon és milyen célsejtekhez jut el. A melittin esetében ezt a kettősséget különösen jól ismerjük: nagyobb koncentrációban membránkárosító, erősen irritáló és citotoxikus lehet, miközben kisebb dózissal több modellben gyulladáscsökkentő jellegű válasz mutatkozott[1], [2], [4], [11].
Az útvonal sem részletkérdés. A bőr felszínére felvitt méhméreges szérum vagy kenőcs egészen más farmakokinetikai helyzetet hoz létre, mint a dermalis, szubkután vagy akupunktúrás pontba adott injekció. A bőr barrier-funkciója természetes szűrő, amely a molekulák egy részét visszatartja, más részét lassabban engedi át, és közben maga is reagál a formulára. Ezért topikális terméknél sokkal nagyobb súlya van a vivőanyagoknak, a bázisnak és az összetevők kombinációjának[5], [12], [14].
A dózis kérdése azért is kulcsfontosságú, mert a méhméreg természetes változékonysága önmagában is befolyásolja a 'valódi' expozíciót. Két azonosnak tűnő készítmény között lehet különbség a melittin arányában, a PLA2-terhelésben vagy az allergénprofilban. Ebből a szempontból a standardizált kivonat vagy a jól dokumentált formuláció nem luxus, hanem alapfeltétel[1], [2], [20].
A gyakorlati következtetés nagyon egyszerű: amikor valaki a 'méhméreg pozitív hatásairól' olvas, mindig tegye hozzá gondolatban ezt a kérdést is - milyen dózisban, milyen készítményben, milyen útvonalon? Ha ez hiányzik egy cikkből vagy termékleírásból, az már önmagában figyelmeztető jel.
Módszertani korlátok: mit nehéz jól mérni?
A méhméreg-kutatás módszertani nehézségeit ritkán tárgyalják a népszerű cikkek, pedig éppen ezek magyarázzák, miért olyan lassú a klinikai előrelépés. Az első probléma a heterogenitás: a vizsgálatok nem ugyanazzal a készítménnyel, nem ugyanazon dózissal, nem ugyanabban a betegcsoportban és nem ugyanazokkal a végpontokkal dolgoznak. Emiatt két pozitív tanulmány sem feltétlenül összegezhető könnyen[2], [5], [7], [9].
A második nagy gond a vakítás és a placebo kérdése. A méhméreg gyakran okoz lokális érzést, melegedést, csípő vagy irritáló reakciót, ami megnehezíti a valódi kettős vak kutatási elrendezést. Ha a résztvevő vagy a kezelő sejti, melyik karban van, az torzíthatja a szubjektív végpontokat, például a fájdalomértékelést. Ez különösen fontos olyan indikációkban, ahol a primer kimenetel eleve önértékelésen alapul[5], [6], [8].
A harmadik probléma a készítményazonosság. Sok tanulmányban nincs részletesen leírva, milyen tisztaságú, milyen feldolgozású, milyen komponensprofilú venomot használtak. A modern farmakológia viszont éppen azt tanítja, hogy egy komplex természetes anyagnál az összetételi bizonytalanság könnyen a reprodukálhatóság rovására megy. Emiatt a jobb minőségű jövőbeli vizsgálatoknak standardizáltabb kémiai és fehérjeprofil-leírásra lesz szükségük[2], [3], [20].
A negyedik nehézség a ritka, de súlyos mellékhatások becslése. Ha egy vizsgálat kicsi, rövid és gondosan válogatott betegeken fut, abból nem lehet megnyugtatóan következtetni arra, mennyire ritka egy valódi élethelyzetben az anafilaxia. Ezért értékesek különösen az allergológiai irányelvek, mert emlékeztetnek rá: a ritka kockázat is kockázat marad, különösen akkor, ha potenciálisan életveszélyes[21], [22], [23].
És van egy ötödik, kommunikációs probléma is: a publikált pozitív eredmények sokkal gyorsabban jutnak el a közönséghez, mint a nulleredmények vagy a negatív vizsgálatok. A tudományban ezt publikációs torzításnak nevezzük. A méhméreg témájában ezért minden lelkesítő eredmény mellé oda kell képzelni a kérdést is: vajon hány hasonló, de kevésbé látványos vizsgálat nem kapott ugyanekkora figyelmet?[7].
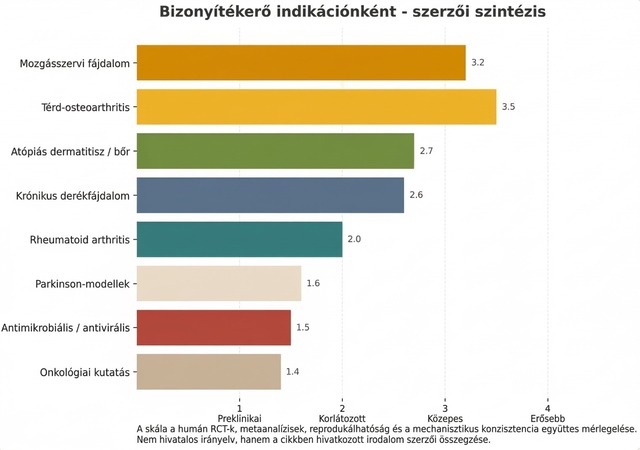
Mozgásszervi fájdalom és osteoarthritis
Ha azt kérdezzük, hol a legerősebb a humán jelzés, a válasz jelenleg a mozgásszervi fájdalom körül keresendő. A 2025-ben közölt metaanalízis húsz randomizált vizsgálatot vont össze a méhméreg pharmacopuncture és rokon beavatkozások témájában, és összességében kedvező fájdalomcsökkenést talált a sham-sóoldatos kontrollokhoz képest. Ugyanakkor a szerzők hangsúlyozták a kis mintaszámot, a heterogén protokollokat és azt, hogy a negatív, nem publikált eredmények torzíthatják az összképet. Magyarul: a jelzés pozitív, de nem végleges[7].
A térdízületi kopással kapcsolatos egyik legnagyobb humán vizsgálatban 538 résztvevőt randomizáltak, és tizenkét heti dermalis kezelés után a méhméreggel kezelt csoportban a WOMAC-alapú fájdalom és funkció szignifikáns javulása volt látható. Különösen érdekes, hogy az injekciós helyi reakciók aránya 5% alatt maradt, az összbiztonsági profil pedig a tanulmány leírása szerint nem mutatott kirívó különbséget a kontrollhoz képest. Ez nem jelenti azt, hogy a kezelés mindenki számára megfelelő, de azt igen, hogy az osteoarthritis vonalon már nem pusztán állatkísérleti szintről beszélünk[6].
A krónikus derékfájdalommal foglalkozó 2017-es, randomizált, kettős vak, sham-kontrollos vizsgálat 54 beteg adatait közölte. Három hét után a bee venom acupuncture csoportban szignifikáns javulást írtak le a fájdalom zavaró voltában, a fájdalomintenzitásban és a funkcionális státuszban. A vizsgálat kis méretű volt, de módszertanilag komolyabb, mint sok korábbi apiterápiás tanulmány, ezért a teljes bizonyítékláncban fontos helyet foglal el[8].
A gyakorlati olvasat itt az, hogy a méhméreg fájdalomcsillapító potenciálja valószínűleg nem légből kapott állítás, de a legjobb adatok jelenleg többnyire injekciós vagy akupunktúrás-szerű alkalmazásokból származnak. Ebből közvetlenül nem következik, hogy bármelyik topikális termék ugyanilyen hatáserővel dolgozik. A bőrön keresztüli hozzáférés, a koncentráció, a vivőanyag és a kontaktidő teljesen más farmakológiai helyzetet teremt[5], [6], [7], [8].
Rheumatoid arthritis: ígéret és korlát
A rheumatoid arthritis különösen jó példa arra, miért kell különválasztani a mechanisztikus izgalmat és a klinikai bizonyosságot. A sejt- és állatkísérletes irodalomban a méhméreg, illetve a melittin több ponton is antiinflammatorikus képet mutat: csökkentheti a gyulladásos mediátorok termelődését, és befolyásolhatja az NF-kB-vezérelt folyamatokat[10], [11].
Mégis, amikor a humán klinikai bizonyítékot nézzük, a 2014-es szisztematikus áttekintés mindössze egy megfelelő RCT-t tudott bevonni, és a szerzők alacsony minőségű bizonyítékról számoltak be. Ez azt jelenti, hogy a rheumatoid arthritis esetében nem lenne tudományosan korrekt erős, általános hatékonysági állításokat tenni. A potenciál jelen van, de a klinikai alátámasztás még sovány[9].
Ez a terület ugyanakkor azért érdekes, mert a rheumatoid arthritis mechanizmuskutatása hozzájárult ahhoz, hogy jobban megértsük a méhméreg immunológiai hatásait. A jövő egyik nagy kérdése itt is az lehet, hogy a teljes venom helyett egy-egy célzott frakció - vagy éppen detoxifikált, standardizált változat - tud-e jobb kockázat-haszon arányt felmutatni[2], [20].
Bőrgyógyászat, atópiás dermatitisz és kozmetológia
A bőrgyógyászati vonal a méhméreg-kutatás egyik legérdekesebb, a vásárlók számára talán leginkább releváns ága. A topikális készítményeknél ugyanis a felhasználás logikája sokkal közelebb áll ahhoz, amit a hétköznapi vásárló ismer: krém, emolliens, szérum, kenőcs. A bizonyítékok itt sem hibátlanok, de több olyan humán adat van, amely miatt a téma komolyan vehető[12], [13], [14].
Egy 136 résztvevős, multicentrikus, kettős vak, randomizált vizsgálatban a méhmérget tartalmazó emolliens az atópiás dermatitiszben szenvedő betegeknél kedvező változást mutatott az EASI-pontszámban és a viszketés vizuális analóg skáláján. Ez fontos eredmény, mert nem laboratóriumi csészében, hanem valós, bőrtünetes embereknél vizsgálták a formulát. Ugyanakkor azt is látni kell, hogy ez egy konkrét készítmény és konkrét vizsgálati protokoll eredménye; ebből nem következik automatikusan, hogy minden méhméreges bőrápoló ugyanezt tudja[12].
Mechanisztikusan a bőrgyógyászati szakirodalom gyakran az NF-kB- és STAT-útvonalak gátlásán, valamint a gyulladásos kemokinek és citokinek csökkentésén keresztül magyarázza a megfigyelt javulást. Atópiás dermatitisz-modellben a bee venom és a melittin csökkentette a bőr gyulladásos jelzéseit, ami szépen összecseng a humán emolliens-vizsgálat által jelzett iránnyal[12], [13].
A kozmetológiai alkalmazások még inkább formulafüggők. Egy kisebb humán vizsgálat szerint bee venom serum használata mellett javultak a finom ráncokkal kapcsolatos paraméterek - terület, szám és mélység -, ami arra utal, hogy megfelelően megtervezett kozmetikai rendszerben a méhméreg a bőr felszíni megjelenésére is hatással lehet. Itt viszont a mértékletesség a kulcs: a kozmetológiai javulás nem azonos gyógyászati állítással, és a készítmény minősége, koncentrációja, valamint a bőrtípus meghatározó tényező[14].
Az olvasó szempontjából a legfontosabb kérdés talán ez: van-e értelme méhméreges krémet vagy kenőcsöt keresni? A tudományos válasz az, hogy igen, bizonyos bőrkomfortot, nyugtató vagy bőrkép-javító célt szem előtt tartva lehet racionális döntés, de csak akkor, ha a termék transzparens, jó minőségű és reális állításokkal kommunikál. Ha ilyen formulákat keres, nézze meg a méhméreges készítmények kategóriáját, és közben tartsa szem előtt: a topikális bőrápolás nem azonos az injekciós terápiával, viszont a bőr mindennapi támogatásában lehet releváns szerepe.
Neurológiai kutatás és Parkinson-modellek
A neurológiai kutatásban a méhméreg különösen a Parkinson-kór modelljeiben kapott figyelmet. Állatkísérletes eredmények szerint a bee venom javíthatja a motoros teljesítményt és mérsékelheti a neuroinflammáció egyes markereit. Egy 2015-ös patkánymodellben a méhméreg enyhítette a motoros deficiteket, és az apamin részben utánozta ezt a hatást, ami az SK-csatornák szerepére utal[15].
Egy másik, alfa-szinuklein transzgenikus egérmodellben a bvPLA2 - a teljes méhméreggel és a melittinnel szemben - különösen érdekes neuroprotektív aktivitást mutatott: a szerzők regulátor T-sejt aktivációt és a Th1/Th17-irány csökkentését írták le. Ez azért jelentős, mert a Parkinson-kór ma már nem pusztán 'dopaminhiányos', hanem erősen neuroimmunológiai szemmel is vizsgált kórkép[16].
Az idegrendszeri terület azonban tipikusan az a mező, ahol a laikus túlértelmezés kockázata a legnagyobb. A jelenlegi adatok alapján nem lenne korrekt azt állítani, hogy a méhméreg bizonyított Parkinson-terápia. A helyes megfogalmazás az, hogy a méhméreg egyes komponensei kutatási szempontból ígéretesek neuroinflammatorikus és neuroprotektív mechanizmusok vizsgálatára, de a humán transzláció még előkészítő szakaszban van[2], [15], [16].
Antimikrobiális és antivirális irányok
Az antimikrobiális és antivirális kutatások mögött elsősorban az a megfigyelés áll, hogy a méhméreg bizonyos komponensei - különösen a melittin - képesek lehetnek a mikrobiális membránok destabilizálására, illetve egyes vírusok életciklusának zavarására. A probléma itt is ugyanaz, mint az onkológiai kutatásban: amit egy baktérium vagy vírus szempontjából előnyösnek látunk, az könnyen lehet túl agresszív az emberi sejteknek is[1], [17].
A 2023-as antivirális áttekintés szerint a méhméreg, a melittin és a PLA2 számos burkos és nem burkos vírus ellen mutatott aktivitást különböző laboratóriumi rendszerekben. A fejlesztési gondolat itt jellemzően nem az, hogy a nyers méhmérget 'gyógyszerként' adjuk, hanem az, hogy a belőle származó molekulákat vagy azok módosított változatait hogyan lehet célzottabb, kevésbé toxikus platformokra ültetni[17].
A baktériumellenes fejlesztésekben jó példa a méhméreggel töltött kitozán nanorészecske-rendszer, amely Staphylococcus aureus ellen erősebb antibakteriális hatást és alacsonyabb citotoxicitást mutatott, mint a natív venom. Az ilyen eredmények azért fontosak, mert a nyers hatóanyag korlátait próbálják mérnöki és gyógyszertechnológiai eszközökkel megkerülni. A valódi innováció tehát sokszor nem maga a méhméreg, hanem a méhméreg intelligens formulálása[18].
Webes szinten ez a rész kifejezetten keresett, mert sok olvasó a 'méhméreg antibakteriális hatása' kulcsszóra jut el egy ilyen cikkhez. Tudományosan viszont fontos kimondani, hogy a jelenlegi klinikai bizonyíték nem elég ahhoz, hogy fertőzések önálló, otthoni kezelésére bárki méhmérget ajánljon. Ami erős: a kutatási irány. Ami gyenge: a rutinszerű humán alkalmazhatóság[17], [18].
Onkológia: miért izgalmas, és miért kell óvatosnak lenni
Az onkológiai kutatás a méhméreg egyik leglátványosabb, ugyanakkor leginkább félreérthető területe. A tudományos irodalomban valóban vannak kifejezetten meggyőző laboratóriumi eredmények: például emlőrák-modellekben a honeybee venom és a melittin gátolta az EGFR- és HER2-jelátvitelt, valamint fokozta a tumorsejtek pusztulását, sőt bizonyos modellrendszerekben a docetaxel hatását is erősítette[19].
Ezek az adatok azonban nem jelentik azt, hogy a méhméreg bizonyított daganatellenes terápia emberekben. Az onkológiai fejlesztés rendkívül magas belépési küszöbű terület, ahol a szelektivitás, a dózis, a szisztémás toxicitás, az immunreakció és a gyógyszerhordozás kérdései mind döntőek. A legtöbb modern cikk ezért már nem a nyers venom közvetlen használatáról, hanem melittin-analógokról, liposzómákról, hidrogélekről, konjugátumokról és más célzott rendszerekről beszél[2], [19].
Az onkológiai tartalom olvasói szempontból ugyan csábító, mert sok kattintást hozhat, de szakmai szempontból itt kell a legfegyelmezettebbnek lenni. A korrekt üzenet így hangzik: a méhméreg tumorbiológiai kutatási platformként ígéretes, és egyes komponensei fontos gyógyszerfejlesztési inspirációt adnak, de ma még nem részei a standard daganatellenes terápiának. A túlzó állítás rövid távon figyelmet szerezhet, hosszú távon viszont rombolja a hitelességet[2], [19].
Topikális termék vagy injekciós megközelítés?
Az egyik leggyakoribb félreértés, hogy a 'méhméreg terápia' és a 'méhméreges krém' ugyanannak a történetnek két neve. Tudományosan ez nem igaz. A bőrre felvitt készítmény és az injekciós vagy akupunktúrás alkalmazás között alapvető különbség van a dózisban, a felszívódásban, a célzott szöveti elérésben és a kockázati profilban is[5], [6], [8], [12].
A topikális termékek világa emiatt inkább a formulációs tudományról szól. Számít, mennyi a valódi méhméreg-tartalom, mennyire standardizált az alapanyag, milyen vivőrendszerben van jelen, milyen egyéb összetevőkkel kombinálták, és milyen bőrtípusra készült. Egy jó méhméreges készítmény nem attól profi, hogy hangosan ígér, hanem attól, hogy átláthatóan kommunikál a koncentrációról, az összetevőlistáról, a felhasználási módról és az óvatossági szempontokról.
| Szempont | Topikális krém / kenőcs / szérum | Injekciós / pharmacopuncture / apipuncture |
|---|---|---|
| Fő cél | Bőrápolás, helyi komfort, kozmetológiai vagy enyhe támogató cél | Fájdalom, gyulladás vagy kutatási/klinikai célú intervenció |
| Felszívódás | Bőrbarrier által erősen szabályozott, formulafüggő | Közvetlenebb szöveti hozzáférés, más biológiai hatásprofil |
| Bizonyítékok | Bőrgyógyászati és kozmetikai vizsgálatokból, készítményspecifikusan | RCT-k és metaanalízisek főként mozgásszervi fájdalomban |
| Kockázat | Kontaktreakció, irritáció, allergia | Lokális reakciók, allergia, ritka súlyos szisztémás reakciók |
| Otthoni használat | Körültekintéssel, termékválasztás és próba alapján lehetséges | Nem otthoni kísérletezésre való, szakmai felügyeletet igényel |
| Kommunikáció | Reális bőrápolási és komfortállítások | Orvosi, kutatási és biztonsági keretek közé helyezendő |
A vásárlói döntésnél különösen sokat számít a transzparencia. Érdemes olyan terméket keresni, amelynél a gyártó nem keveri össze a kozmetológiai nyelvet a gyógyszerészeti állításokkal, és nem sugallja azt, hogy egy krém automatikusan helyettesíthet klinikai kezeléseket. Ha a cél bőrápolás, komfortérzet, masszázs utáni nyugtatás vagy célzott, helyi rutin kialakítása, akkor a topikális megközelítés logikus lehet. Ha viszont valaki injekciós vagy apipunktúrás jellegű kezelést keresne, annak már teljesen más biztonsági kapun kell átmennie[12], [14], [21], [22].
Sok olvasó számára innen válik a tudomány gyakorlattá: mitől jó egy méhméreges kenőcs? Röviden attól, hogy korrekt forrásból származik, világos az INCI-listája, jó a bőrérzet, nem dolgozik irreális ígéretekkel, és a gyártó jelzi a próbahasználat szükségességét. A minőségi szűréshez kiindulópont lehet a méhméreg, méhmérges kenőcs és krém kategória, ahol a topikális felhasználás logikájával érdemes nézni a termékeket - nem pedig az injekciós szakirodalmat egy az egyben rájuk húzni.
Milyen topikális terméktípusok léteznek?
A topikális világon belül sem mindegy, milyen hordozóformáról beszélünk. A méhméreg önmagában nem 'krém' vagy 'kenőcs', hanem hatóanyag-jellegű komponens. A készítmény karakterét végső soron az alapformula adja meg: olajosabb balzsam, víz-olaj emulzió, könnyű szérum vagy gyors beszívódású gél.
| Terméktípus | Tipikus felhasználás | Előny | Korlát / megjegyzés |
|---|---|---|---|
| Krém | Mindennapi bőrápolás, célzott helyi rutin | Kiegyensúlyozott textúra, gyakran kényelmesebb érzékenyebb bőrre | A hatás a teljes formulától függ, nem csak a méhméregtől |
| Kenőcs / balzsam | Masszázs, szárazabb területek, védőbb érzet | Tartósabb filmréteg, hosszabb helyi kontaktidő | Zsírosabb érzet, nem minden bőrtípus kedveli |
| Szérum | Arcbőr, könnyebb textúra, kozmetológiai rutin | Gyorsabb beszívódás, rétegezhetőség | Érzékeny bőrön a koncentrált aktívanyag-környezet miatt óvatos bevezetés kell |
| Gél | Frissítő, gyors felszívódású helyi használat | Könnyű érzet, praktikus sport vagy nyári rutin mellett | A hidratáló-komfort változó lehet |
A megfelelő terméktípus kiválasztásánál ezért nemcsak azt kell nézni, hogy 'van-e benne méhméreg', hanem azt is, hogyan illeszkedik a bőrtípushoz, a napi rutinhoz és a használat céljához. Egy arcbőrre szánt szérum és egy masszázshoz használt kenőcs nem felcserélhető kategóriák.
Vásárlói ellenőrzőlista
A tudatos vásárlás a méhméreges készítményeknél többet jelent annál, mint hogy 'van-e benne méhméreg'. A kérdés inkább az, hogy a teljes készítmény mennyire koherens, mennyire átlátható, és mennyire tiszteli a felhasználó biztonságát.
Gyors ellenőrzőlista méhméreges krém vagy kenőcs választásához
- Van egyértelmű INCI-lista és legalább alapvető gyártói transzparencia.
- A kommunikáció nem ígér gyógyulást minden problémára, hanem pontosan leírja a felhasználási célt.
- A méhméreg szerepe nem puszta marketingdísz, hanem a készítmény logikájába illeszkedik.
- Az első használat előtt indokolt a kis területen végzett próba.
- Érzékeny, ekcémás vagy sérült bőr esetén fokozott óvatosság szükséges.
- Korábbi méhcsípés-allergia esetén a termékválasztás előtt szakmai egyeztetés javasolt.
A hitelesség egyik ismertetőjele, hogy a gyártó nem próbálja elmosni a különbséget a kozmetikum, a wellness-jellegű termék és az orvosi kezelés között. Ez üzleti szempontból is fontos: a túlzó ígéretek rövid távon kattintást hozhatnak, de hosszú távon bizalomvesztéshez vezetnek.
Mítoszok és tények a méhméregről
A méhméreg témája körül rengeteg a leegyszerűsítő mondat. Az alábbi párok segítenek gyorsan szétválasztani a félreértéseket a tudományosan védhető állításoktól.
Mítosz: ami természetes, az biztonságos is.
Tény: a méhméreg természetes eredetű, de bizonyos embereknél súlyos, akár életveszélyes allergiás reakciót válthat ki. A természetes eredet legfeljebb a forrást írja le, nem a kockázatot[21], [22], [23].
Mítosz: a méhméreg minden gyulladásos betegségre bizonyított megoldás.
Tény: vannak ígéretes gyulladáscsökkentő mechanizmusok és néhány pozitív humán vizsgálat, de az indikációk között óriási a különbség. Ami osteoarthritisben vagy dermatitiszben bíztató, az nem jelenti automatikusan, hogy más betegségekben is bizonyított[6], [7], [9], [12].
Mítosz: a méhméreges krém ugyanaz, mint a méhméreg-terápia.
Tény: a topikális készítmény és az injekciós alkalmazás eltérő farmakológiai és biztonsági kategória. A klinikai bizonyítékok jelentős része nem kozmetikai krémekből, hanem injekciós protokollokból származik[5], [6], [8], [12].
Mítosz: a rákellenes laboreredmény már majdnem klinikai bizonyíték.
Tény: a sejt- és állatkísérletes onkológiai eredmények fontosak, de a klinikai út nagyon hosszú. A szelektivitás, a toxicitás és a célba juttatás problémája itt meghatározó[19].
Kockázatok, allergia és ellenjavallatok
A méhméreggel kapcsolatos legfontosabb ellenpont az allergia kérdése. A Hymenoptera-venom allergia potenciálisan életveszélyes lehet, és a szakirodalom szerint a szisztémás allergiás reakciók gyakorisága a felnőtt populációban akár 7,5%, gyermekeknél pedig körülbelül 3,4% is lehet. Ez azt jelenti, hogy bármilyen méhméreggel kapcsolatos kommunikáció szakmailag csak akkor tekinthető korrektnek, ha a pozitív hatások mellé a ritka, de súlyos kockázatokat is odateszi[21], [22], [23].
Az allergológiában a méhméreg egészen más szerepben jelenik meg, mint az apiterápiás vagy kozmetológiai irodalomban. Itt a standardizált venom immunotherapy - VIT - célja éppen a jövőbeli szisztémás reakciók megelőzése. Az irányelvek szerint a fenntartó dózis rendszerint 100 mikrogramm, bizonyos helyzetekben 200 mikrogramm is lehet. Ebből az olvasó számára az a tanulság, hogy az allergia kezelése nem házi kísérletezés, hanem szoros, szakellátási protokoll[21], [22].
A biztonság kérdését tehát legalább három szinten kell nézni. Első: allergia - lehet-e túlérzékenység? Második: lokális tolerancia - hogyan reagál a bőr vagy a kezelt terület? Harmadik: termékminőség - valóban standardizált, tiszta és átlátható formuláról beszélünk-e? Ez a háromszög sokkal fontosabb, mint bármilyen hangzatos marketingmondat[2], [20], [21], [22], [23].
| Rizikóhelyzet | Miért fontos? | Óvatos megközelítés |
|---|---|---|
| Korábbi szisztémás reakció méhcsípésre | Az anafilaxia kockázata miatt ez a legerősebb vörös zászló. | Ne kísérletezzen otthon, kérjen allergológiai véleményt. |
| Ismert méhméreg-allergia | A 'kis dózis' sem garantál biztonságot, az útvonal és az egyéni érzékenység számít. | Topikális használat előtt is orvosi egyeztetés javasolt. |
| Erősen reaktív, sérült vagy ekcémás bőr | Az irritáció és a kontaktreakció valószínűsége nőhet. | Kis felületen próba, fokozatos bevezetés, rosszabbodás esetén leállítás. |
| Otthoni injekciós gondolat | A dózis, a sterilitás és a súlyos reakciók kezelése szakmai környezetet igényel. | Nem javasolt, nem tekinthető biztonságos házi megoldásnak. |
| Túlzó marketingígéretek | A valós bizonyítékoknál erősebb állítások félrevezethetnek. | Keresse az átlátható, bizonyíték-arányos kommunikációt. |
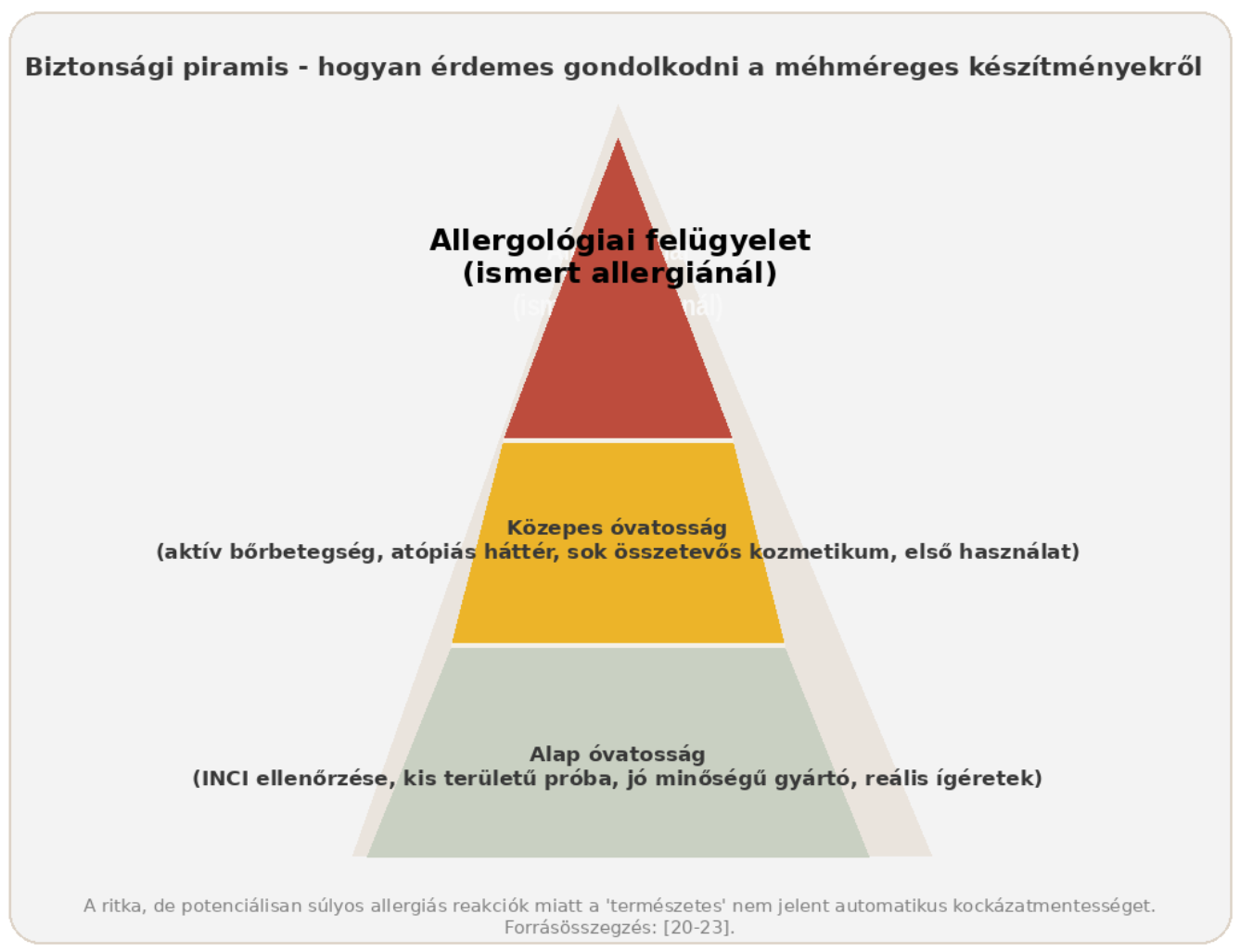
Topikális készítményeknél a legésszerűbb minimum a kis felületen végzett próbahasználat és az INCI-lista tudatos átnézése. Injekciós, szúrásos vagy otthon improvizált megoldások viszont nem tekinthetők felelős útnak. Ha valakinek korábban már volt általános tünete méhcsípés után - légszomj, kiterjedt csalánkiütés, szédülés, eszméletvesztésközeli állapot -, akkor a méhméreggel kapcsolatos bármely további lépést kizárólag allergológiai értékelés előzheti meg[21], [22], [23].
Standardizálás, minőség és fenntarthatóság
A méhméreg-kutatás egyik legnagyobb, laikus szemmel kevésbé látványos, de döntő fontosságú témája a standardizálás. A venom összetétele változhat méhpopuláció, szezon, takarmányozási háttér, gyűjtési technika, szárítás és tárolás szerint. Ez azt jelenti, hogy két 'méhméreges' termék névleg ugyanabba a kategóriába tartozhat, miközben a biológiai valóságban egészen más rendszerek[1], [2], [3], [4].
A modern kutatás ezért egyre inkább a standardizált, tisztított, sőt részben detoxifikált készítmények felé mozdul. A 2021-es vizsgálat szerint a detoxified bee venom csökkent citotoxicitást és allergenitást mutatott, miközben az antiinflammatorikus aktivitás fennmaradt vagy akár fokozódott. Ha ez a fejlesztési vonal beigazolódik, az jelentősen javíthatja a kockázat-haszon arányt[20].
A minőség másik oldala az etika. Bár a korszerű gyűjtési rendszerek nem feltétlenül rontják a kolóniák teljesítményét vagy áttelelési esélyét, a mérsékelt stresszválasz ténye arra emlékeztet, hogy a méhméreg nem egyszerű alapanyag. A felelős méhészeti gyakorlat, az ésszerű gyűjtési intenzitás és a nyomon követhetőség mind hozzátartozik ahhoz, hogy egy ilyen termékkategória hosszú távon hiteles maradjon[2], [4].
Merre tart a kutatás?
A jövő nagy valószínűséggel nem a nyers méhméreg diadala lesz, hanem a precíziós méhméreg-alapú fejlesztéseké. Ez több irányt jelent egyszerre: tisztított frakciók, például bvPLA2 vagy melittin célzott vizsgálata; toxikológiailag optimalizált, detoxifikált változatok; valamint olyan gyógyszerhordozó rendszerek, amelyek a hatóanyagot a megfelelő helyre juttatják el, miközben védik a környező egészséges szöveteket[2], [17], [18], [19], [20].
Különösen érdekesek a nanotechnológiai megközelítések. Ha a melittin vagy más peptidek önmagukban túl agresszívek, akkor az egyik fejlesztési út az, hogy hordozóhoz kötve, célzott felszabadítással, környezetfüggő aktiválással használjuk őket. Ez a gondolkodás már most is jelen van az onkológiai és antimikrobiális irodalomban, és várhatóan a bőrgyógyászati formulációkban is egyre hangsúlyosabb lesz[18], [19].
Ugyanilyen fontos trend a bizonyítékok minőségének javítása. Több nagyobb, jobban standardizált, transzparens RCT-re van szükség, különösen topikális készítmények, mozgásszervi indikációk és hosszabb távú biztonság témájában. A méhméreg-kutatás akkor léphet igazán előre, ha a következő években nemcsak több, hanem módszertanilag is jobb humán vizsgálat születik[6], [7], [12], [21].
Végső következtetések
A modern szakirodalom alapján a méhméreg nem divatszó, és nem is egyszerű népi folklór. Valós bioaktív rendszer, amelynek gyulladáscsökkentő, fájdalommoduláló, immunológiai és bőrgyógyászati jelentősége tudományosan egyre jobban körvonalazódik. A legerősebb humán jelek ma bizonyos mozgásszervi fájdalomkórképekben és egyes bőrgyógyászati alkalmazásokban látszanak, miközben a neurológiai, antivirális és onkológiai vonal inkább kutatási távlatként tekinthető[2], [6], [7], [8], [12], [15], [17], [19].
Ha egyetlen mondatban kellene összefoglalni a lényeget, így hangzana: a méhméreg pozitív hatásai valósak lehetnek, de csak akkor értelmezhetők helyesen, ha a bizonyíték szintjét, az alkalmazás formáját és a kockázatokat egyszerre nézzük. Ez a hozzáállás nem gyengíti, hanem erősíti a hitelességet - és hosszú távon pontosan ez az, amit az olvasó és a kereső is értékel.
Topikális nézőpontból a legérettebb üzenet nem az, hogy a méhméreg mindenre jó, hanem az, hogy megfelelő minőségű, átgondolt formulákban helye lehet a modern bőrápolási és komfortorientált rutinban. Ha pedig valaki tovább böngészne a témában, a méhméreges krémek és kenőcsök kategóriája jó gyakorlati belépési pont lehet ehhez a tudatos, árnyalt szemlélethez.
Gyakori kérdések
Mi az a méhméreg, és miben különbözik a propolisztól vagy a méztől?
A méhméreg - apitoxin - a háziméh védekező váladéka, amely peptidek, enzimek és kisebb bioaktív molekulák keveréke. A propolisz növényi gyantákból származó kaptáranyag, a méz pedig a nektárból készülő élelmiszer. A három anyag biológiailag és felhasználásában is teljesen eltérő világot képvisel[1], [2], [3].
Mely pozitív hatásokat támasztja alá leginkább a tudomány?
Jelenleg a mozgásszervi fájdalom egyes formái, például térd-osteoarthritis vagy krónikus derékfájdalom, valamint bizonyos bőrgyógyászati alkalmazások mutatják a legerősebb humán jelet. A Parkinson-kór, az onkológia és az antivirális terület többnyire még preklinikai szinten ígéretes[6], [7], [8], [12], [15], [17], [19].
Egy méhméreges krém ugyanazt tudja, mint az injekciós méhméreg-terápia?
Van-e értelme méhméreges kenőcsöt használni bőrre?
Kiknek kell különösen óvatosnak lenniük?
Miért olyan fontos a standardizálás?
Mit jelent az, hogy detoxified bee venom?
A detoxifikált méhméreg olyan feldolgozott forma, amelyben a fejlesztők igyekeznek csökkenteni a citotoxicitást és az allergénterhelést, miközben a kedvező biológiai aktivitás megmarad. Ez a kutatási irány a jövőben sokat javíthat a biztonsági profilon[20].
Gyógyítja-e a méhméreg a rákot vagy a Parkinson-kórt?
Fogalomtár
- Apitoxin
- A méhméreg tudományos megnevezése.
- Melittin
- A méhméreg legnagyobb mennyiségben jelen lévő, erősen bioaktív peptidje.
- PLA2
- Foszfolipáz A2; enzim, amely egyszerre lehet allergén és immunmodulátor kutatási célpont.
- NF-kB
- Olyan transzkripciós szabályozó rendszer, amely számos gyulladásos gén működését irányítja.
- IKK
- Az NF-kB aktivációjának fontos enzimegyüttese.
- COX-2
- Gyulladásos prosztaglandinok képződésében részt vevő enzim.
- iNOS
- Indukálható nitrogén-oxid-szintáz; gyulladásos folyamatokban gyakran fokozódik.
- Treg
- Regulátor T-sejt; az immunválasz fékezésében és egyensúlyában fontos szereplő.
- Th1 / Th17
- Gyulladásos immunválaszokban részt vevő T-sejtes mintázatok.
- Pharmacopuncture
- Olyan gyakorlat, amely injekciós készítményt kombinál akupunktúrás pontokkal.
- EASI
- Eczema Area and Severity Index; atópiás dermatitisz súlyosságának egyik mértéke.
- WOMAC
- Osteoarthritisben használt tünet- és funkciómérő kérdőív.
- Anafilaxia
- Gyorsan kialakuló, potenciálisan életveszélyes szisztémás allergiás reakció.
- Detoxified bee venom
- Olyan módosított méhméreg-készítmény, amelynek toxikusságát és allergenitását csökkenteni próbálják.
- SK-csatorna
- Kis vezetőképességű kalciumaktivált káliumcsatorna; idegrendszeri kutatásokban fontos molekuláris célpont.
Melléklet: evidenciamátrix és háttérolvasmányok
Az alábbi mátrix gyors áttekintést ad arról, hogy a méhméreggel kapcsolatos fő területek milyen bizonyítéki szinten állnak, melyek a fő korlátok, és milyen gyakorlati következtetés vonható le belőlük. A cél nem a túlértékesítés, hanem a tiszta, bizonyítékarányos eligazítás.
| Indikáció / terület | Bizonyíték típusa | Mit mutatnak az adatok? | Fő korlát | Szerzői összegzés | Fő források |
|---|---|---|---|---|---|
| Térd-osteoarthritis | Humán RCT, nagyobb minta | Jelentős WOMAC-javulás 12 hetes kezeléssel | Dermalis/injekciós protokoll, nem topikális | Ígéretes, de formuláció- és protokollfüggő | 6 |
| Krónikus derékfájdalom | Humán RCT | Fájdalom és funkció javulása 3 hét alatt | Kis minta, rövid utánkövetés | Valós fájdalomcsillapító jelzés | 8 |
| Mozgásszervi fájdalom összességében | Metaanalízis | Összességében kedvező fájdalomcsökkenés | Heterogén vizsgálatok | Közepes erejű, fejlődő bizonyíték | 7 |
| Rheumatoid arthritis | Szisztematikus áttekintés | Humán adat kevés | Egyetlen kis RCT, alacsony minőség | Mechanisztikusan érdekes, klinikailag még gyenge | 9-11 |
| Atópiás dermatitisz | Humán RCT + preklinikai háttér | EASI és viszketés javulása emollienssel | Készítményspecifikus eredmény | Topikális irányban komolyan vehető | 12-13 |
| Facial wrinkles / kozmetológia | Kis humán vizsgálat | Ráncparaméterek javulása | Kis minta, kozmetológiai végpontok | Óvatosan optimista | 14 |
| Parkinson-modellek | Állatkísérletek | Motoros és neuroinflammatorikus javulás | Humán transzláció hiányzik | Kutatási platform | 15-16 |
| Antiviral / antibacterial | Preklinikai | Membránkárosító és formulációs előnyök | Humán bizonyíték elégtelen | Innovációs irány, nem rutinterápia | 17-18 |
| Onkológia | Preklinikai / transzlációs | Tumorsejt-ellenes aktivitás és jelátviteli gátlás | Szelektivitás és toxicitás kritikus | Látványos laboreredmények, de nem kész klinikum | 19 |
| Biztonság / allergia | Irányelvek, áttekintések | Súlyos reakció ritka, de valós veszély | Egyéni kockázat nagyon eltérő | Minden kommunikáció központi része kell legyen | 21-23 |
Közérthető háttérolvasmányok és további, a témát különböző mélységben tárgyaló oldalak:
- A méhméreg és főbb összetevőinek terápiás alkalmazásai
- Átfogó ismertető a méhméreg gyógyászati felhasználásáról
- Természetes megközelítés a gyulladásos és fertőző betegségek ellen
- A méhméreg terápia egészségügyi előnyei és kockázatai
- Klinikai kutatások a méhméreg orvosi célú felhasználásáról
- A méhméreg farmakológiai tulajdonságainak újabb vizsgálatai
- UCLA Health: A méhméreg ígéretes jövője a gyógyításban
- Tudományos alapok az apiterápiához
- Bőrgyógyászati és kozmetológiai alkalmazások
- A méhméreg molekuláris szintű hatásmechanizmusai
Kulcspublikációk rövid kommentárral
Ha valaki a teljes irodalomjegyzék helyett néhány irányadó forrásból indulna el, az alábbi rövid kommentár segíthet. Ez a rész kifejezetten a gyors szakmai tájékozódást szolgálja.
| Kulcspublikáció | Miért fontos? | Forrás |
|---|---|---|
| Wehbe és mtsai. 2019 | Alapvető nyílt hozzáférésű áttekintés a méhméreg fő komponenseiről és bioaktivitásairól. | 1 |
| Stela és mtsai. 2024 | Friss, széles panorámájú review a terápiás potenciálról és mechanizmusokról. | 2 |
| Sung és mtsai. 2025 | Hasznos metaanalízis a mozgásszervi fájdalom humán eredményeiről. | 7 |
| Conrad és mtsai. 2019 | Kiemelt osteoarthritis-RCT, nagy mintával. | 6 |
| You és mtsai. 2016 | A topikális, atópiás dermatitiszes vonal egyik legfontosabb humán vizsgálata. | 12 |
| Duffy és mtsai. 2020 | Onkológiai laboreredmény, amelyet sokan idéznek - fontos, de nem humán terápia. | 19 |
| Rueff és mtsai. 2023 / Sturm és mtsai. 2018 | Allergológiai irányelvek; a biztonsági fejezet kulcsforrásai. | 21-22 |
Irodalomjegyzék
- Wehbe R, Frangieh J, Rima M, El Obeid D, Sabatier JM, Fajloun Z. Bee Venom: Overview of Main Compounds and Bioactivities for Therapeutic Interests. Molecules. 2019;24(16):2997.
- Stela M és mtsai. Therapeutic Potential and Mechanisms of Bee Venom Therapy in Human Diseases. Pharmaceuticals. 2024;17(9):1211.
- Khalil WKB, Assaf N, ElShebiney SA, Salem NA. Bee Venom: From Venom to Drug. Molecules. 2021;26(16):4941.
- Ullah A és mtsai. Pharmacological properties and therapeutic potential of honey bee venom. Saudi Pharmaceutical Journal. 2023;31:101692.
- Sung WS, Lee JH. Bee Venom Acupuncture for Pain and Its Mechanisms: An Updated Review. Toxins. 2021;13(9):608.
- Conrad A és mtsai. Bee Venom for the Treatment of Knee Osteoarthritis: A Randomized, Double-Blinded, Controlled Trial. Journal of Alternative and Complementary Medicine. 2019.
- Sung WS és mtsai. Effectiveness and safety of bee venom pharmacopuncture for musculoskeletal pain: a systematic review and meta-analysis of randomized controlled trials. BMC Complementary Medicine and Therapies. 2025.
- Seo BK és mtsai. Bee Venom Acupuncture for Chronic Low Back Pain: A Randomized, Double-Blinded, Sham-Controlled Trial. Toxins. 2017;9(11):361.
- Lee MS, Pittler MH, Shin BC, Kong JC, Ernst E. Bee venom acupuncture for rheumatoid arthritis: a systematic review of randomised clinical trials. BMJ Open. 2014;4:e006140.
- Park HJ és mtsai. Antiarthritic effect of bee venom: inhibition of inflammation mediator generation by suppression of NF-kappaB through interaction with the p50 subunit. Arthritis and Rheumatism. 2004;50(11):3504-3515.
- Park HJ és mtsai. Melittin inhibits inflammatory target gene expression and mediator generation via interaction with IkappaB kinase. British Journal of Pharmacology. 2007;150(4):409-421.
- You CE és mtsai. Effects of Emollient Containing Bee Venom on Atopic Dermatitis: A Double-Blinded, Randomized, Base-Controlled, Multicenter Study. Annals of Dermatology. 2016;28(5):593-599.
- An HJ és mtsai. Anti-inflammatory effects of bee venom and melittin on atopic dermatitis through blockade of NF-kappaB and STAT signaling pathways. British Journal of Pharmacology. 2018.
- Han SM és mtsai. The effect of bee venom serum on facial wrinkles: a clinical study. Clinical Interventions in Aging. 2015;10:1587-1592.
- Maurice T és mtsai. Bee venom alleviates motor deficits and modulates neuroinflammatory responses in rat models of Parkinson's disease. PLoS One. 2015;10:e0142838.
- Ye M és mtsai. Bee venom phospholipase A2 ameliorates motor dysfunction and modulates neuroinflammation in alpha-synuclein transgenic mice. Experimental and Molecular Medicine. 2016;48:e244.
- Yaacoub S és mtsai. Bee Venom and Its Derived Components against Viruses: A Review. Pathogens. 2023;12(11):1354.
- Sameh YS és mtsai. Enhanced antibacterial activity of bee venom-loaded chitosan nanoparticles against Staphylococcus aureus with reduced cytotoxicity. Scientific Reports. 2023.
- Duffy C és mtsai. Honeybee venom and melittin suppress growth factor receptor activation and induce cell death in HER2-enriched and triple-negative breast cancer. npj Precision Oncology. 2020;4:24.
- Lee G és mtsai. Detoxified bee venom reduces allergenicity and cytotoxicity while retaining or enhancing anti-inflammatory activity. Applied Biochemistry and Biotechnology. 2021.
- Rueff F és mtsai. Diagnosis and treatment of Hymenoptera venom allergy: German guideline update. Allergologie Select. 2023.
- Sturm GJ és mtsai. EAACI guidelines on allergen immunotherapy: Hymenoptera venom allergy. Allergy. 2018;73(4):744-764.
- Kamga GPF és mtsai. Prevention of Hymenoptera venom anaphylaxis. Current Opinion in Allergy and Clinical Immunology. 2024.







